La coagulación en el tratamiento de aguas
El agua y las aguas residuales pueden contener impurezas suspendidas y disueltas que deben ser eliminados para cumplir con ciertos criterios de calidad de agua. Estas impurezas incluyen:
- Limo
- Bacterias, algas y virus
- Material derivado de materia orgánica del suelo
- Sustancias minerales
- Contaminantes industriales, etc.
Las impurezas suspendidas y disueltas pueden ser clasificadas según su diámetro:
| Tipo de impureza | Diámetro (m) |
| Sólidos suspendidos | > 10-3 |
| Sólidos coloidales | 10-9– 10-6 |
| Sólidos disueltos | <10-9 |
Una partícula con un diámetro mayor de 10-5 m sedimentará dentro de un tiempo razonable.
Diámetro (m) Tipo de partícula * Tiempo de sedimentación de 30 cm
| Diámetro (m) | Tipo de partícula | * Tiempo para sedimentar 30 centímetros |
| 10-2 | Grava | 0,3 segundos |
| 10-3 | Arena gruesa | 3 segundos |
| 10-4 | Arena fina | 38 segundos |
| 10-5 | Limo | 33 minutos |
| 10-6 | Bacterias | 35 horas |
| 10-7 | Arcilla | 230 días |
| 10-8 | Coloide | 63 años |
Sin embargo, el tiempo de sedimentación de las partículas coloidales incluso puede alcanzar años.
La filtración, como la filtración rápida en arena, puede no eliminar dichas impurezas de manera eficiente, sin un tratamiento previo de coagulación y floculación.
El propósito del proceso de coagulación y floculación es crear partículas pequeñas y suspendidas, crear flóculos y aumentar su tamaño para que puedan sedimentarse o eliminarse por filtración.
Mira la vista previa de la clase sobre coagulación y floculacción del curso online «Tratamiento de aguas»:
Coagulación y floculacción – vista previa
Información sobre el curso en tratamiento de aguas
[visual-link-preview encoded=»eyJ0eXBlIjoiZXh0ZXJuYWwiLCJwb3N0IjoxMzUzNywicG9zdF9sYWJlbCI6IlBhZ2UgMTM1MzcgLSBMb3MgZnVuZGFtZW50b3MgZGUgdHJhdGFtaWVudG8gZGUgYWd1YXMiLCJ1cmwiOiJodHRwczovL2Nyb3BhaWEuY29tL2VzL2Z1bmRhbWVudG9zLXRyYXRhbWllbnRvLWFndWFzP2tleTE9Y29hZyIsImltYWdlX2lkIjoxMzQyMiwiaW1hZ2VfdXJsIjoiaHR0cHM6Ly9jcm9wYWlhLmNvbS93cC1jb250ZW50L3VwbG9hZHMvTG9zLWZ1bmRhbWVudG9zLWRlLXRyYXRhbWllbnRvLWRlLWFndWFzLW1vY2t1cC5wbmciLCJ0aXRsZSI6IkxvcyBmdW5kYW1lbnRvcyBkZSB0cmF0YW1pZW50byBkZSBhZ3VhcyIsInN1bW1hcnkiOiJFbCBsaWJybyBMb3MgZnVuZGFtZW50b3MgZGUgdHJhdGFtaWVudG8gZGUgYWd1YXMgbGUgbGxldmEgYSB0cmF2w6lzIGRlIGxhIHRlb3LDrWEgeSBsYSBwcsOhY3RpY2EgZGUgbG9zIHByb2Nlc29zIGRlIHRyYXRhbWllbnRvIGRlIGFndWFzLlxuXG5FbiBlc3RlIGxpYnJvIHJlY2nDqW4gcHVibGljYWRvLCBhcHJlbmRlcsOhIGxvcyBmdW5kYW1lbnRvcyBkZWwgdHJhdGFtaWVudG8gZGUgYWd1YXMgeSBsb3Mgw7psdGltb3MgYXZhbmNlcyB0ZWNub2zDs2dpY29zLiBFbCBhdXRvciBleHBsaWNhIGxhcyBkaWZlcmVudGVzIG9wZXJhY2lvbmVzIHVuaXRhcmlhcywgc3VzIHBhcsOhbWV0cm9zIGRlIGRpc2XDsW8geSBjb25zaWRlcmFjaW9uZXMgb3BlcmF0aXZhcywgYXPDrSBjb21vIGxhcyBwcsOhY3RpY2FzIGFjdHVhbGVzLCBsYXMgcHJlb2N1cGFjaW9uZXMgZW1lcmdlbnRlcyB5IGxvcyByZXF1aXNpdG9zIHJlZ2xhbWVudGFyaW9zLiBUb2RvIGV4cGxpY2FkbyBkZSB1bmEgbWFuZXJhIGbDoWNpbCBhIGxlZXIsIHBhcmEgcXVlIHB1ZWRhIHRlbmVyIHVuYSBjb21wcmVuc2nDs24gY2xhcmEgZGUgY2FkYSB0ZWNub2xvZ8OtYS4gSGFnYSBjbGljIGFxdcOtIHBhcmEgbcOhcyBpbmZvcm1hY2nDs24uIiwidGVtcGxhdGUiOiJ1c2VfZGVmYXVsdF9mcm9tX3NldHRpbmdzIn0=»]
¿Qué es la coagulación en el tratamiento de aguas?
La coagulación es un proceso químico en el que se agrega un compuesto químico, un «coagulante”, al agua, para desestabilizar las partículas suspendidas y promover la formación de flóculos.
Una «partícula coloidal estable» es una partícula coloidal que permanece como una entidad separada en el agua, es decir, en un estado disperso.
La razón por la cual las partículas coloidales tienden a permanecer dispersas es porque su superficie está cargada eléctricamente, generalmente con una carga negativa.
Las cargas superficiales de las partículas forman una «doble capa eléctrica»: los iones positivos en la solución de agua se acercan a la partícula con carga negativa y se concentran en su superficie. La concentración de estos contraiones se reduce con la distancia de la superficie de la partícula. A medida que cargas similares se repelen entre sí, esta distribución de carga genera fuerzas de repulsión que evitan que las partículas se acerquen entre sí.
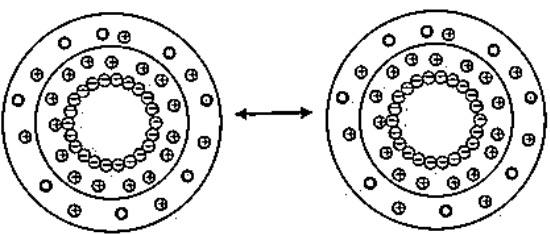
Dos partículas con doble capa eléctrica
Los mecanismos de coagulación
Los coagulantes actúan en cuatro mecanismos diferentes, que pueden actuar individualmente, o simultáneamente:
- Compresión de la doble capa.
- Adsorción electrostática.
- Adsorción y puente.
- Precipitación o coagulación de barrido.
Compresión de la doble capa eléctrica: Puede ocurrir cuando se introducen electrolitos. Una mayor concentración de electrolitos neutraliza más cargas y, como resultado, el espesor de la doble capa eléctrica se reduce y las partículas se acercan entre sí.
Adsorción electrostática: neutralización de la carga superficial del coloide. Esto resulta en la reducción del potencial de superficie y en la desestabilización del coloide. Este mecanismo generalmente ocurre cuando se introducen coagulantes inorgánicos, como alumbre o sulfato ferroso.
Adsorción y puente: una molécula puente (un polímero) adsorbe una partícula coloidal a un sitio activo y otra partícula coloidal a otro sitio. Este puente produce una formación de un flóculo más grande. El coagulante podría ser un polímero orgánico natural o un polímero sintético.

Coagulación de barrido: Adición de dosis relativamente alta de coagulante, generalmente sales de aluminio o hierro, puede resultar en precipitación de los óxidos del metal hidratado, debido a la limitación de su solubilidad.
Las partículas coloidales quedan atrapadas en el precipitante a medida que sedimenta y se asientan con él.
Tipos de coagulantes utilizados en el tratamiento de agua y aguas residuales:
Los coagulantes se pueden clasificar como coagulantes orgánicos y coagulantes inorgánicos.
Los coagulantes orgánicos son polímeros catiónicos de alto peso molecular. La principal ventaja de los coagulantes orgánicos es que producen mucho menos lodo que los coagulantes inorgánicos, debido a su mayor eficacia. Otra ventaja es que no afectan el pH del agua tratada.
Los coagulantes orgánicos incluyen poliaminas, poliDADMACS, diciandiamida y melamina formaldehído.
Los coagulantes inorgánicos se basan principalmente en sales metálicas, como el sulfato de hierro y el sulfato de aluminio. Cuando se introducen en el agua, reaccionan con la alcalinidad del agua e hidratan para formar un hidróxido de metal.
Su reacción con el agua disminuye la alcalinidad y el pH del agua, por lo tanto, ajuste de la alcalinidad puede ser necesario.
Los coagulantes inorgánicos producen lodo debido a la precipitación del hidróxido de metal y la materia coloidal. También aumentan los sólidos disueltos totales en el agua. Por ejemplo, como resultado de la adición de sulfato con sulfato de aluminio.
Se pueden formar diferentes hidróxidos metálicos, dependiendo del coagulante que se esté usando, de la alcalinidad del agua y el pH. El tipo de hidróxido de metal que se forma afecta en gran medida el proceso de coagulación. Por lo tanto, cada coagulante tiene un rango de pH óptimo en el cual funciona mejor.
Por ejemplo, el alumbre funciona mejor a un pH de entre 5,8 y 6,5, el clorhidrato de aluminio (ACH) funciona a un rango de pH de entre 6,5 y 7,5.
¿Cómo elegir un coagulante?
La elección del coagulante dependerá de varios factores, que incluyen:
- La dosis requerida
- Precio y disponibilidad
- El pH del agua
- El efecto del coagulante sobre el pH y la alcalinidad
- Eficiencia para parámetros requeridos específicos
- Corrosividad
Para elegir el mejor coagulante, o una mezcla de coagulantes, para el agua específica que se va a tratar, se debe realizar una prueba de jarra. La prueba jarra estándar se realiza en un laboratorio, utilizando 6 vasos, cuando en cada vaso se prueban diferentes condiciones. Modificando las condiciones del proceso – la dosificación, el pH, el tiempo de coagulación, el tiempo de sedimentación, la energía de agitación etc., se pueden determinar las condiciones óptimas.





