El pH del suelo
El grado de acidez o alcalinidad del suelo se expresa en unidades de pH. El pH del suelo afecta a muchos procesos, incluidos la disponibilidad de los nutrientes de las plantas, la actividad de microorganismos y el desarrollo de las raíces de la planta.
En suelos naturales, el pH suele oscilar entre 4,5 y 8,0. Los suelos con pH de 6,5 a 7,5 se consideran neutros, suelos con pH inferior a 6,5 se consideran ácidos y suelos con pH superior a 7,5 se consideran alcalinos. La mayoría de los nutrientes vegetales están disponibles a un pH ligeramente ácido de 5,8 a 6,5.
Descarga Gratuita - El paquete técnico para los agrónomo y productores
Conversión de unidades, interpretación de análisis de suelos, de agua y más
El efecto del pH de suelo en la disponibilidad de nutrientes
A un pH del suelo inferior a 5.2, los nutrientes como el calcio, magnesio, nitrógeno, fósforo y boro pueden dejar de estar disponibles para las plantas. Sin embargo, la solubilidad y disponibilidad de micronutrientes, como el hierro, aluminio, manganeso, zinc y cobre aumentan significativamente y puede volverse tóxico.
En suelos muy ácidos, el proceso de mineralización de la materia orgánica se ralentiza e incluso puede detenerse por completo ya que la actividad microbiana disminuye en condiciones de pH bajo. Esto resulta en una menor disponibilidad del nitrógeno y fósforo.
En suelos de pH alto, las deficiencias de micronutrientes se vuelven comunes.
La disponibilidad de fósforo se reduce tanto en suelos muy ácidos, con pH inferior a 5,5, como en suelos alcalinos con pH superior a 7,5. En suelos ácidos, el fósforo reacciona con el hierro y el aluminio y deja de estar disponible, mientras que, en suelos alcalinos, el calcio se fija el fósforo y lo hace menos disponible por la formación de compuestos de insolubles fosfatos de calcio.
Los suelos alcalinos se caracterizan por la presencia de carbonatos de calcio, magnesio y sodio. A un pH de entre 7,2 y 8,2, el suelo está dominado por carbonatos de calcio y magnesio y el suelo se denomina «suelo calcáreo». A un pH del suelo por encima de 8,2, el suelo está dominado por carbonatos de sodio, ya que se vuelven altamente solubles. Altos niveles altos de sodio en relación con el calcio y el magnesio pueden afectar negativamente la estructura del suelo.
La disponibilidad de nutrientes a diferentes niveles de pH se describe en la siguiente figura. Cuanto más gruesa sea la barra, más disponible estará el nutriente.
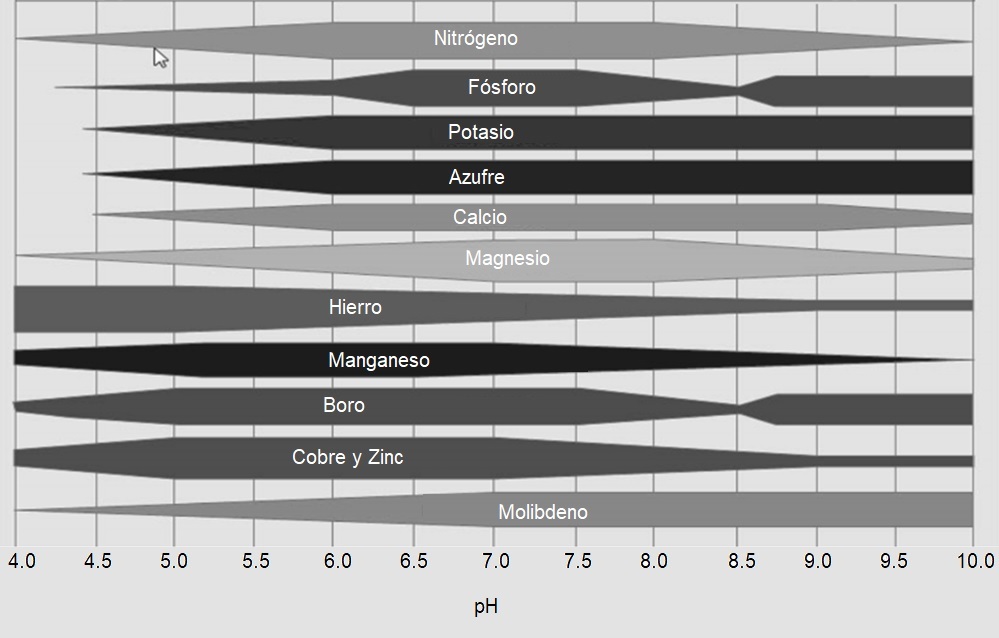 Disponibilidad de nutrientes en función del pH
Disponibilidad de nutrientes en función del pH
Fertilización y Riego - Teoría y Mejores Prácticas
El libro, escrito por el ing. Guy Sela, cubre la teoría y práctica de manejo de la nutrición vegetal y el riego – las dos prácticas más importantes en la producción de cultivos. Todo explicado en una manera clara fácil de leer. Haga clic aquí para más información.
Tipos de acidez del suelo
Fuentes de acidez Hay tres tipos de acidez en el suelo: la acidez activa, acidez intercambiable y acidez residual.
La acidez activa es la concentración de iones de hidrógeno libres (H+) en la solución del suelo. El pH del suelo es una medida de la acidez activa del suelo.
La acidez intercambiable se refiere a los iones de hidrógeno y aluminio retenidos en el complejo de intercambio del suelo, es decir, sobre las superficies de los coloides del suelo. Es la acidez potencial del suelo, debido a que los iones del aluminio (Al3+) y del hidrógeno (H+) retenidos, están en equilibrio con la solución del suelo, junto con los iones de calcio (Ca2+), magnesio, (Mg2+), potasio (K+) y sodio (Na+).
Cuanto mayor sea la capacidad de intercambio catiónico del suelo, mayor será su capacidad amortiguadora, ya que el suelo puede retener una mayor cantidad de iones de hidrógeno y aluminio en su complejo de intercambio.
La capacidad amortiguadora del suelo se refiere a su capacidad para resistir cambios de pH. Dado que la acidez activa está en equilibrio con la acidez intercambiable, los iones de aluminio e hidrógeno adsorbidos pueden reponer el aluminio y el hidrógeno que se eliminaron de la solución del suelo. Por lo tanto, los suelos con alta CIC y pH bajo requerirán más cal para aumentar el pH de suelo al nivel deseado.
Mientras que el calcio, magnesio, potasio y sodio se consideran cationes básicos, el aluminio y el hidrógeno se consideran ácidos.
El aluminio se considera ácido debido a las reacciones de hidrólisis que ocurren en la solución del suelo. La hidrólisis del aluminio genera iones de hidrógeno, es decir acidez activa.
Al3+ + H2O = Al(OH)2+ + H+
Al(OH)2+ + H2O = Al(OH)2+ + H+
Al(OH)2+ + H2O = Al(OH)3 + H+
Al(OH)3 + H2O = Al(OH)4– + H+
La acidez residual se asocia con iones de aluminio e hidrógeno que están unidos a los coloides del suelo, pero no de forma intercambiable.
La determinación del pH del suelo
Existen varios métodos para determinar el pH de suelo. Todos los métodos miden la acidez activa, es decir, los iones de hidrógeno en la solución del suelo. Sin embargo, cada método proporcionará resultados diferentes para la misma muestra de suelo. Por lo tanto, para interpretar correctamente los resultados, es importante comprender la diferencia entre los métodos.
Los métodos basados en extracción de agua:
- pH del extracto de la pasta saturada
- pH de extracto 1: 2 (1 parte de suelo, 2 partes de agua)
- Extracto 1: 5 (1 parte de suelo, 5 partes de agua)
Cuanta más agua se use para la extracción, mayor será el pH medido, ya que la adición de agua diluye los iones de hidrógeno en el extracto.
En los métodos que utilizan solo agua para la extracción, los iones de hidrógeno que están adsorbidos a las superficies de las partículas del suelo permanecen adsorbidos y no se liberan en la solución.
Los métodos que utilizan agente químico para la extracción:
Para obtener un resultado que represente mejor las condiciones de campo, se usa comúnmente una solución diluida de cloruro de potasio (KCl 1,0 M) o cloruro de calcio (CaCl2 0,01 M). La concentración de sal en las soluciones pretende representar la concentración de sal en la solución del suelo. El potasio o el calcio en las soluciones de extracción reemplazan algunos de los iones de hidrógeno adsorbidos a las partículas del suelo y, por lo tanto, el pH medido con estos métodos suele estar más cerca del pH real del suelo.
Las lecturas de pH medido en KCl o CaCl2 son de 0,5 a 1,5 unidades más bajas que el pH medido en agua, debido a la mayor concentración de iones de hidrógeno en la solución extraída.
Plataforma agronómica basada en IA
Plataforma agronómica basada en IA
Descubra yieldsApp, la plataforma agronómica líder en el sector que está revolucionando la forma en que los agricultores y agrónomos gestionan sus cultivos. Con nuestra avanzada tecnología basada en inteligencia artificial, le ofrecemos herramientas y soluciones para optimizar la fertilización, la salud del suelo, el manejo de cultivos y el manejo de plagas y enfermedades.
- Disña programas de fertilización
- Interpreta los análisis de suelo, agua y análisis foliares
- Recomienda tratamientos contra plagas y enfermedades
- Proporciona herramientas para el monitoreo de cultivo (imágenes satelitales, modelos de cultivos y más)
- ¡Disponible en esáñol!
- Obtenga su prueba gratuita aquí






